
헌팅턴병 치료제 컨퍼런스 2018 – 3일차
헌팅턴병 치료제 컨퍼런스 3일차 업데이트: 헌팅틴 단백질 – 그리고 수치 낮추기
2018 HD 치료제 컨퍼런스 마지막 날 아침이야! 오늘은 두 세션이 있는데, 첫 번째는 HD 유전자에서 만들어지는 단백질에 초점을 맞추고 있어. 두 번째는 Wave Life Sciences와 Ionis Pharmaceuticals의 헌팅틴 수치 감소 임상 시험에 대한 업데이트를 포함하고 있어.
목요일 아침 – 헌팅틴 단백질
모든 HD 환자는 동일한 돌연변이, 즉 C-A-G 서열의 길이가 길어진 것을 물려받았어. 이 확장은 우리가 지금 HD 유전자라고 부르는 유전자에서 발생해. 유전자는 세포가 단백질을 만드는 지침으로 사용되는데, 오늘 첫 번째 세션은 HD 단백질에 초점을 맞추고 있어.

그르노블 알프스 대학교의 산드린 험버트(Sandrine Humbert)는 뇌 발달과 HD 유전자 및 단백질이 이 과정에 미치는 영향에 오랫동안 관심을 가져왔어. 이 과정을 이해하기 위해 험버트 연구실은 뇌에서 HD 유전자와 단백질이 없는 생쥐를 만들었어. 그들은 HD 유전자가 없는 세포가 비정상적으로 분열하고 이동한다는 것을 발견했어. 뇌 발달 중에 새로 태어난 세포는 종종 다른 세포가 형성한 ‘밧줄’을 따라 기어 올라가면서 적절한 위치로 이동해. HD 유전자가 제거되면 이 과정이 변경되는데, 이는 HD 유전자가 이 과정에서 중요한 역할을 한다는 것을 시사해.
IRBM 사이언스 파크의 안드레아 카리카솔(Andrea Caricasole)은 헌팅틴 단백질의 “번역 후 변형”에 대한 대규모 연구를 진행하고 있어. 이는 헌팅틴 단백질의 미세한 화학적 “장식”을 의미해. 이러한 장식은 세포가 단백질의 기능을 조절할 수 있게 해줘. 예를 들어, 헌팅틴 단백질은 수십 개의 이러한 태그가 추가되고 제거되면서 다양한 신호에 반응하여 헌팅틴의 기능을 조절하는 것으로 보여. 이러한 장식 중 많은 부분이 헌팅틴 단백질에 흥미로운 영향을 미치며, 심지어 돌연변이 헌팅틴 단백질이 세포를 손상시키는 것을 막을 수도 있어. 우리는 이전에 HDBuzz에서 이에 대해 썼어. 카리카솔 팀은 개별 헌팅틴 단백질 장식에 대한 매우 민감한 테스트를 개발하고 있어. 이를 통해 질병 과정에서 어떤 것들이 변하는지 추적하고, 어쩌면 그것들을 고칠 방법을 찾을 수도 있을 거야.
워싱턴 대학교의 로히트 파푸(Rohit Pappu)는 헌팅틴 단백질을 이해하는 데 매우 집중적인 접근 방식을 취하고 있어. 그의 연구실은 HD 돌연변이에 의해 모양이 영향을 받는 단백질 부분을 연구하기 위한 도구를 개발하고 있어. 파푸 연구실은 엄청난 양의 컴퓨터 파워를 사용하여 돌연변이에 의해 변형된 헌팅틴 단백질 부분의 모양을 예측하려고 해. 이러한 기술을 통해 그들은 “올챙이” 모양을 관찰할 수 있어. 이 올챙이 모양은 HD 분야에서 치열한 논쟁의 대상이었어! 파푸의 기술은 이 논쟁의 한쪽을 강력하게 지지하며, 이는 헌팅틴 단백질의 이 중요한 부분을 더 잘 이해하는 데 도움이 될 거야.
에모리 대학교의 샤오-장 리(Xaio-Joang Li)는 성체 생쥐의 뇌, 몸 또는 둘 다에서 헌팅틴 유전자를 끌 수 있는 흥미로운 생쥐 모델을 개발했어. 이 생쥐들은 확장된 헌팅틴 유전자를 가지고 있지 않아. 단지 ‘건강한’ 버전의 유전자를 끄는 것이 어떤 결과를 초래하는지 이해하는 데 도움이 될 뿐이야. 다행히도 유전자를 껐을 때 뇌에서는 나쁜 일이 일어나지 않았어. 예상치 못하게 유전자를 끄면 췌장에 염증이 생겼어. 이것이 환자에게 어떤 의미를 가질지는 불분명하지만, 현재의 헌팅틴 수치 감소 치료법은 뇌뿐만 아니라 몸 전체의 헌팅틴 수치를 크게 줄일 것으로 예상되지는 않아. 리 박사는 또한 CRISPR-Cas9 유전자 편집을 사용하여 생쥐의 HD 유전자에서 유해한 부분을 잘라냈어. 생쥐에서 돌연변이 유전자를 비활성화하자 독성 헌팅틴 단백질 형성이 성공적으로 감소했고, 생쥐들도 더 잘 움직였어. 리 박사는 정말 바빴어! 그는 또한 CRISPR 유전자 편집을 사용하여 헌팅턴병 모델 돼지를 만들었어. 돼지 뇌가 인간과 유사하기 때문에 새로운 약물 테스트에 유용할 수 있을 거야.
“코하넥은 단백질을 얼리고 전자빔을 사용하여 수천 장의 사진을 찍었어. 그런 다음 컴퓨터로 결합하여 헌팅틴 단백질의 상세한 분자 구조를 보여주는 최초의 사진을 만들었어.”
@UCSanDiego의 안쿠르 자인(Ankur Jain)은 RNA를 연구하는데, RNA는 세포가 DNA의 지침을 사용하여 단백질을 만들고 싶을 때 생성되는 “메시지 분자”야. 우리의 DNA는 세포 핵에 살지만, RNA는 세포 전체에 자유롭게 떠다녀. 많은 유전성 뇌 질환에 대한 전통적인 생각은 독성 단백질에 의해 발생한다는 것이지만, 때로는 돌연변이 유전자에서 생성되는 RNA 메시지 분자도 독성이 있을 수 있다는 증거가 늘고 있어. 예를 들어, 일부 RNA 서열은 중요한 단백질 기계에 달라붙어 세포에서 제 역할을 하지 못하게 할 수 있어. 독성 RNA의 한 가지 가능한 징후는 HD 및 기타 뇌 질환에서 세포에서 보이는 비정상적인 RNA 덩어리의 형성이야. 자인은 RNA를 젤리처럼 가열하고 식힘으로써 인공 RNA 덩어리를 형성할 수 있다는 것을 발견했어. 이 덩어리들은 HD의 CAG 확장과 같은 끈적한 서열을 RNA가 포함할 때만 형성돼. 이러한 RNA 덩어리가 HD에서 해를 끼치는지 여부는 불분명하지만, 그럴 수도 있어. 예를 들어, RNA가 핵에 갇히면 단백질을 생성하는 데 사용될 수 없어. 안티센스 분자(현재 HD 인간 임상 시험 중인 것과 유사한)는 핵의 RNA에 달라붙어 덩어리 형성을 막을 수 있어. 다른 약물도 이론적으로 뇌 질환의 RNA 끈적임 문제를 해결하는 데 사용될 수 있을 거야.
스테판 코하넥(Stefan Kochanek)의 흥미로운 최신 발표가 있었는데, 그의 연구실은 방금 헌팅틴 단백질의 구조를 밝혀냈어! 단백질이 어떻게 생겼는지 알아내는 것은 단백질이 어떻게 작동하고 약물로 어떻게 변화시킬 수 있는지 이해하는 데 정말 중요한 단계야. 헌팅틴 유전자는 25년 전에 발견되었지만, 단백질은 크고 흔들리고 끈적거려서 구조를 밝히기가 정말 어려웠어. 한 팀은 심지어 결정을 형성하기 위해 단백질을 우주로 보냈지만, 소용이 없었어. 코하넥 팀은 다른 팀들이 실패한 곳에서 성공했고, 그들의 결과는 방금 Nature에 발표되었어. 가장 큰 돌파구는 HAP40(“헌팅틴 관련 단백질 40”)이라는 다른 단백질을 사용하여 헌팅틴을 안정화시킨 것이었어. HAP40으로 안정화된 후, 코하넥은 단백질을 얼리고 전자빔을 사용하여 수천 장의 사진을 찍었어. 그런 다음 컴퓨터로 결합하여 헌팅틴 단백질의 상세한 분자 구조를 보여주는 최초의 사진을 만들었어. 이건 정말 멋진 일이고, 우리가 연구할 수 있는 엄청난 양의 자료를 제공해. 하지만 한 가지 주의할 점은, 일부 영역은 여전히 너무 흔들려서 구조를 파악할 수 없었다는 거야. 여기에는 돌연변이를 포함하는 단백질의 가장 중요한 시작 부분이 포함돼.
목요일 오후 – 헌팅틴 수치 감소
헌팅틴 수치 감소 치료법에 대한 세션이 시작되면서 하루와 컨퍼런스가 성대하게 마무리되고 있어. 헌팅틴 수치 감소는 헌팅틴 단백질 수치를 낮추는 것을 목표로 하는 접근 방식을 의미해. 이를 수행하는 방법은 많지만, 그 중 많은 부분이 HD 유전자의 정보와 헌팅틴 단백질 사이의 중간체인 “RNA”를 표적으로 삼고 있어.
UC 버클리의 마이클 레이프(Michael Rape)는 세포가 세포 내 개별 단백질을 파괴하도록 속이는 데 관심이 있어. HD를 포함한 많은 경우에 특정 단백질 하나를 선택적으로 제거하는 것이 정말 도움이 될 거야. 세포에는 하나 이상의 단백질 분해 경로가 있는데, 중요한 경로는 “유비퀴틴”이라는 작은 화학적 장식을 라벨로 사용해. 세포는 유비퀴틴을 일종의 “나를 먹어라” 신호로 인식하고 이를 운반하는 단백질을 분해해. 레이프 연구실은 세포가 유비퀴틴 태그를 사용하여 매우 빠르게 파괴되어야 하는 단백질(예를 들어 독성이 있을 수 있는 단백질)을 라벨링하는 방법을 이해하는 데 참여해 왔어. 레이프 연구실은 연구자들이 처음으로 단백질이 이 빠른 파괴 경로를 거치는 것을 볼 수 있는 도구를 만들었어. 빠른 단백질 파괴를 위한 기계는 강력한 도구이며, 레이프 연구실은 이를 활용하는 데 관심이 있어. 최근에 개발된 “PROTAC”이라는 기술은 연구자들이 유비퀴틴 시스템을 활용하여 세포가 특정 단백질을 파괴하도록 유도할 수 있게 해줘.
버지니아 대학교의 스콧 자이틀린(Scott Zeitlin)은 HD 생쥐를 대상으로 돌연변이 헌팅틴, 정상 헌팅틴 또는 둘 다를 낮출 때 어떤 일이 일어나는지 알아내려고 노력하고 있어. 각 사람은 부모로부터 하나의 헌팅틴을 물려받으며, HD 환자의 대부분은 하나의 정상 복사본과 하나의 돌연변이 복사본을 가지고 있다는 점을 명심해. 과학자들은 건강한/정상 단백질을 “야생형”이라고 부르는데, 이는 야생에서 더 흔하기 때문이야. 이러한 질문들은 모든 헌팅틴 수치 감소 치료법이 뇌에 있는 헌팅틴 단백질의 전체 양을 줄이는 것을 목표로 하기 때문에 중요해. Ionis의 약물과 같은 일부는 두 가지 버전의 단백질을 동일하게 줄여. Wave의 약물과 같은 다른 약물은 돌연변이 단백질을 야생형 단백질보다 더 많이 낮추는 것을 목표로 해. 우리는 돌연변이 단백질만 낮추거나 야생형 단백질과 병행하여 낮추는 것이 유익할 가능성이 높다고 생각하지만, 헌팅틴 수치를 낮추는 것이 안전한지는 여전히 미해결 질문이야. 자이틀린은 생쥐가 완전히 성장한 후 돌연변이, 야생형 또는 두 단백질의 생산을 줄일 수 있는 생쥐를 사육했어. 자이틀린은 돌연변이 헌팅틴을 조기에 낮추는 것이 뇌에서 단백질 축적 측면에서 더 큰 효과를 가졌다는 것을 발견했어. 마찬가지로, 돌연변이 헌팅틴의 조기 감소는 생쥐의 체중 감소 및 운동 능력에 더 큰 이점을 가져왔어. 두 가지 버전의 단백질 생산을 줄이는 경우에도 마찬가지였어. 조기 치료가 더 큰 이점을 가졌어. 결론은 헌팅틴을 억제하는 데 있어서는 빠를수록 좋다는 거야. 한 가지 테스트(악력)에서는 돌연변이 단백질만 낮추는 것이 성능을 향상시켰지만, 두 가지 버전을 모두 억제하는 것은 그렇지 않았어. 그 외에는 두 가지 접근 방식이 거의 동일하게 효과적이었고, 핵심 요소는 치료가 얼마나 일찍 시작되었는지였어. 자이틀린은 또한 헌팅틴이 다시 증가하도록 허용하면 어떤 일이 일어나는지 살펴보았는데, 이는 생쥐에게 나쁜 영향을 미쳤어. 이는 단기 치료보다 장기 치료가 더 좋다는 것을 시사하며, 이는 예상했던 바와 같아.
OHSU의 조디 맥브라이드(Jodi McBride)는 뇌세포에 자체 RNA 파괴 분자를 만들도록 돕는 지침을 전달하기 위해 무해한 바이러스를 사용하는 그녀의 연구를 설명하고 있어. 이러한 접근 방식의 한 가지 이점은 바이러스가 RNA 파괴 분자를 이론적으로 영원히 만들 수 있게 하여 한 번의 치료로 끝낼 수 있다는 거야. 맥브라이드는 그녀의 치료법을 원숭이에게 전달하여 연구하고 있는데, 원숭이는 우리와 훨씬 더 유사한 크고 복잡한 뇌를 가지고 있어. 특히, 그녀의 팀은 바이러스를 “피각”이라고 불리는 뇌의 한 부분에 전달하는 작업을 하고 있어. 피각은 HD에서 가장 취약한 뇌 영역 중 하나이기 때문에 특히 흥미로워. HD 돌연변이를 물려받은 사람들에게서 상당한 위축이 발생하기 때문이야. 맥브라이드는 주사가 진행되는 동안 뇌를 영상화하기 위해 MRI를 사용하는 것을 포함하여 바이러스 전달에 필요한 뇌 수술의 개선 사항을 설명하고 있어. 바이러스 치료는 피각 전체에서 HD 유전자 RNA를 약 절반으로 감소시켰는데, 이는 이전 시도보다 눈에 띄게 개선된 결과야. 다음은 Wave Life Sciences의 마이크 판자라(Mike Panzara)인데, 그는 HD를 위한 “안티센스 올리고뉴클레오타이드”(ASO)를 사용하는 2가지 임상 시험을 계획하고 있어. ASO는 짧고 변형된 DNA 조각으로, 세포에 들어가 표적 RNA를 파괴하여 표적 단백질의 수치를 줄여.
판자라는 Wave가 현재 HD 환자를 대상으로 ASO 임상 시험 두 가지를 진행 중이라고 군중에게 말했어. 왜 두 가지일까? Wave의 접근 방식은 HD 유전자 내의 “SNP” 또는 “스닙”이라고 불리는 미세한 유전적 변이를 표적으로 삼는 데 의존해. 이러한 미세한 변이는 HD를 유발하지 않아. 단지 사람들 사이의 정상적인 유전적 변이의 일부일 뿐이야. 우리가 모두 일란성 쌍둥이가 아닌 이유이기도 해. 흥미롭게도 이러한 변이는 각 사람이 가지고 있는 HD 유전자 2개 복사본 중 하나에서만 발견돼. 이러한 변이를 표적으로 삼음으로써 Wave의 ASO는 HD 유전자의 돌연변이 복사본과 비돌연변이 복사본을 구별할 수 있어. Wave는 현재 PRECISION-HD1 및 PRECISION-HD2라고 불리는 연구에서 2가지 ASO에 대한 초기 단계 안전성 연구를 진행하고 있어. 이 연구에 사용된 ASO는 HD 유전자 내의 다른 유전적 변이를 표적으로 삼아. 이 접근 방식의 핵심은 사람들이 HD 돌연변이를 물려받았을 뿐만 아니라, 돌연변이 유전자 복사본을 고유하게 표적으로 삼을 수 있는 동반 변이를 가지고 있어야 한다는 거야. 따라서 이러한 임상 시험은 필연적으로 이러한 변이를 가진 환자에게 초점을 맞추고 있어. Wave는 이러한 변이를 감지하고, 어떤 변이가 정상 복사본이 아닌 HD 유전자 돌연변이 복사본에 있는지 결정하는 정말 멋진 신기술을 개발했어. Wave는 예비 연구를 수행하여 자원자의 64%에서 ASO의 표적을 찾을 수 있었어.
“타브리지 박사가 첫 연구에 참여한 용감한 자원자들에게 “진정한 연구 영웅”이라고 칭하며 감사 인사를 전하자 자발적인 박수가 터져 나왔어.”
다음으로, Ionis의 앤 스미스(Anne Smith)와 UCL의 사라 타브리지(Sarah Tabrizi)가 HD 유전자의 두 복사본을 모두 표적으로 하는 ASO를 테스트하기 위해 고안된 임상 시험 결과를 발표하고 있어. 이는 수년간의 노력의 결실이야. 스미스는 Ionis 프로그램이 2005년에 시작되었다는 것을 청중에게 상기시켜 주었어! 그들은 세포 및 동물 연구로 시작하여 ASO 치료가 헌팅틴 단백질을 감소시키고 HD 유사 증상을 개선한다는 초기 증거를 제공했어. 2012년과 2013년에는 헌팅틴 수치를 낮추는 것이 HD 유사 증상을 개선한다는 것을 입증한 HD 생쥐 모델 연구 결과가 발표되었어. 스미스는 @ionispharma가 돌연변이 복사본뿐만 아니라 HD 유전자의 두 복사본을 모두 표적으로 하는 ASO를 사용하기로 결정한 논리를 설명하고 있어. ASO의 한 가지 이점은 뇌 전체에 널리 분포한다는 거야. 스미스는 척수액에 주사한 후 ASO가 뇌 전체에 매우 널리 분포한다는 것을 보여주는 원숭이 실험 데이터를 보여주고 있어. Ionis는 또한 돼지와 같은 더 큰 동물에서도 분포를 연구하여 약물이 매우 널리 분포한다는 것을 발견했어. 그런 다음 독성 연구가 수행되었는데, 이는 약물의 장기 투여가 매우 잘 견뎌진다는 것을 시사했어(원숭이 연구에서는 15개월까지). ASO로 치료받은 환자의 뇌 조직을 채취하는 것은 거의 불가능해. 그렇다면 ASO가 제 역할을 했는지 어떻게 알 수 있을까? 스미스는 뇌의 헌팅틴 수치 감소와 척수액의 헌팅틴 수치 감소 사이의 관계를 확립하는 원숭이 연구를 설명하고 있어. 이를 통해 Ionis는 뇌와 척수액에서 얼마나 많은 헌팅틴 수치 감소가 일어나고 있는지 예측하는 매우 복잡한 컴퓨터 프로그램을 만들 수 있었어. 척수액은 요추 천자를 통해 쉽게 접근할 수 있어. 이 시점에서 Ionis는 ASO에 대한 복잡한 인간 임상 시험을 수행할 자원과 경험을 가진 대형 제약 파트너인 Roche와 합류했어.
사라 타브리지(Sarah Tabrizi)가 무대에 올라 Ionis/Roche의 ASO 치료법에 대한 첫 번째 인간 임상 시험을 설명하고 있어. 이 연구는 “안전성” 연구였어. 연구의 주된 목적은 약물이 안전한지 확인하는 것이었어. 이 연구는 영국, 독일, 캐나다의 9개 지역에서 수행되었어. ASO는 “점증 용량”으로 척수액에 주입하여 환자에게 투여되었는데, 이는 초기 피험자들은 낮은 용량을, 나중 피험자들은 더 높은 용량을 받았다는 의미야. 이러한 신중한 용량 증가는 연구와 독립적인 의사들이 안전성 평가를 수행할 수 있도록 하기 위한 것이었어. 이 연구에는 약물에 처음 노출되는 위험을 감수할 의지가 있는 46명의 놀랍도록 용감한 자원자들이 참여했어. 연구자들은 척수액에서 헌팅틴 단백질 수치를 측정할 수 있었는데, 이는 이전에 뇌 수치와 매우 잘 상관관계가 있다는 것을 보여주었어(뇌 수치는 직접 측정할 수 없다는 것을 기억해).
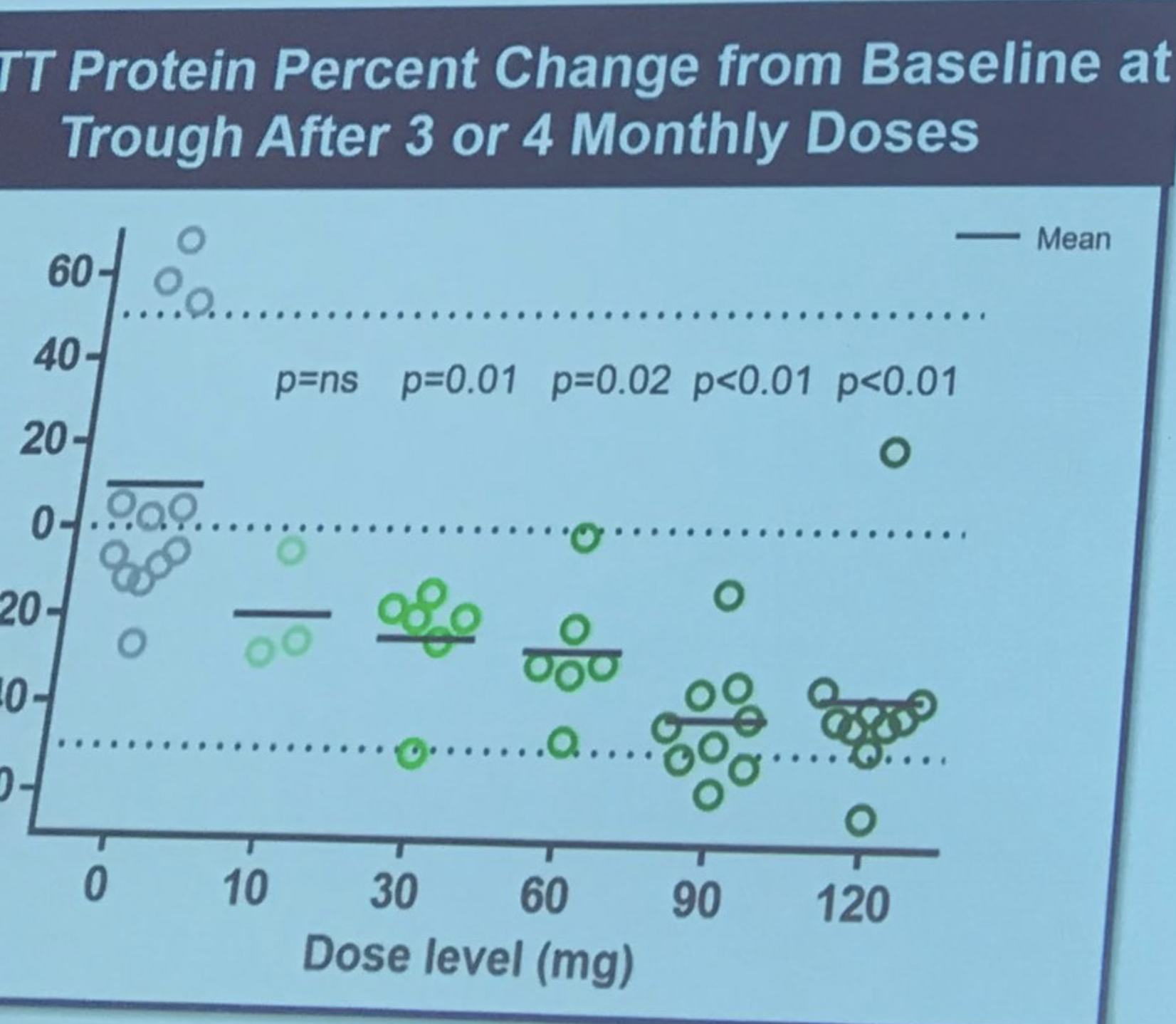
감소 폭은 정말 놀라워. 평균적으로 40-50%에 달해! 타브리지는 헌팅틴 수치 감소가 최대 6개월까지 계속 개선될 수 있다는 연구자들의 느낌을 설명하고 있어. 그리고 타브리지가 예측하는 뇌 단백질 감소량은 다음과 같아. Ionis는 척수액과 뇌 조직의 헌팅틴 수치 감소 사이의 관계를 예측할 수 있는 일종의 모델을 만들었어. 이는 뇌 조직의 헌팅틴 수치 감소가 상당히 높을 수 있음을 시사해. 환자들은 안전을 위해 매우 신중하게 모니터링되었으며, 주요 부작용은 발견되지 않았어. 타브리지 – “이 약물은 테스트된 모든 용량에서 안전하고 잘 견뎌졌어.” 성공이야! 연구의 모든 피험자들은 현재 “공개 라벨 연장”이라고 불리는 단계에 있어. 위약 그룹은 약물 치료로 전환되어 계속 모니터링될 거야. 타브리지가 첫 연구에 참여한 용감한 자원자들에게 “진정한 연구 영웅”이라고 칭하며 감사 인사를 전하자 자발적인 박수가 터져 나왔어.
회의를 마무리하는 정말 멋진 방법이야. Roche와 Ionis가 다음 임상 시험을 계획하면서 앞으로 엄청나게 흥미로운 시간이 될 거야. 다음 임상 시험은 더 많은 사람들에게 약물이 HD 증상을 개선하는지 여부를 결정하도록 설계될 거야.
업데이트: Ionis의 결과에 대한 커뮤니티 성명.



