
강력한 메시지: 독성 RNA 메시지 분자가 헌팅턴병에 해를 끼칠까?
헌팅턴병의 일부 문제가 해로운 단백질 때문이 아니라 다른 것 때문이라면 어떨까?
연구자들은 오랫동안 헌팅턴병 유전자가 세포에 해로운 단백질을 만들라고 지시하여 문제를 일으킨다고 믿어왔어. 스페인 연구자들의 흥미로운 새로운 동물 연구는 헌팅턴병 돌연변이로 인한 문제를 완전히 해결하려면 한 가지 이상의 용의자를 살펴봐야 할 수도 있음을 시사해.
생물학의 중심 원리
모든 헌팅턴병 환자는 어머니나 아버지로부터 물려받은 동일한 기본적인 유전적 돌연변이를 가지고 있어. 이 돌연변이는 간단하게 헌팅턴병 유전자라고 부르는 유전자에 있어.
헌팅턴병을 유발하는 돌연변이는 헌팅턴병 유전자 내 이미 반복적인 DNA 구간이 확장된 것이야. 유전자 한쪽 끝에서 우리는 C-A-G라는 유전적 문자가 계속해서 반복되는 것을 발견할 수 있어. 헌팅턴병이 없는 사람들의 헌팅턴병 유전자에는 이 CAG 서열이 약 20회 반복돼. 하지만 39회 이상 반복되는 헌팅턴병 유전자 사본을 물려받으면, 인생의 어느 시점에서 헌팅턴병이 발병할 거야.
유전자는 세포에 의해 단백질을 만드는 지시, 즉 레시피로 사용돼. 단백질은 세포가 작동하게 하는 기계야. 우리 세포가 할 수 있는 모든 멋진 일들은 각 세포 안에서 빠르게 움직이고 회전하는 수천 가지 다른 단백질들의 복잡한 상호작용에 달려 있어.
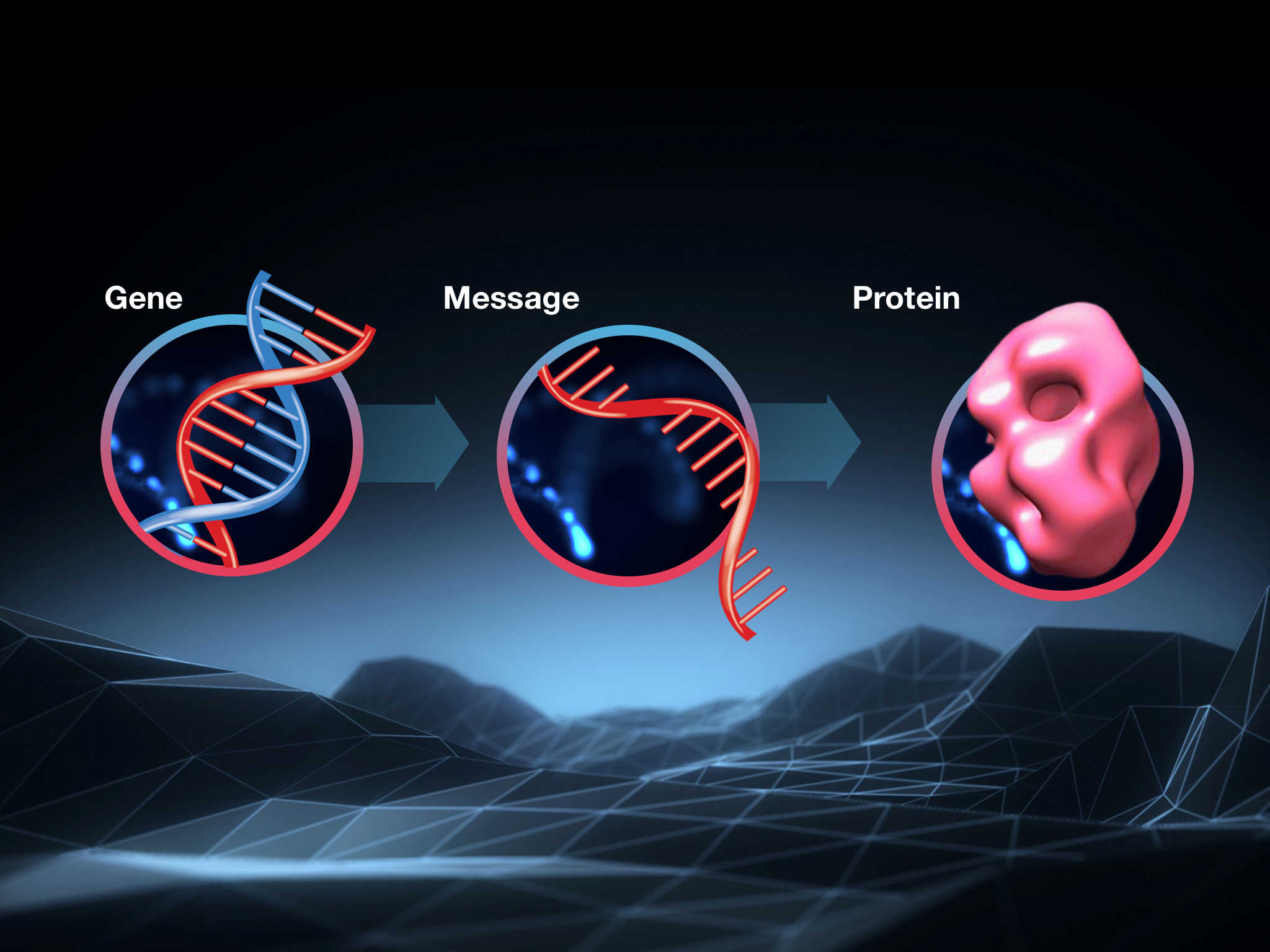
우리 유전자 속 지시와 세포 전체에서 일을 하는 단백질 사이에는 중간 단계가 있어. DNA는 매우 중요하고 어떤 대가를 치르더라도 보호되어야 하기 때문에, 세포가 특정 단백질의 사본을 필요로 할 때, 세포는 그 지시를 RNA라고 불리는 새로운 분자로 복사해.
세포 내 한 곳에서 다른 곳으로 정보를 전달하기 때문에, 과학자들은 이 작업 사본들을 ‘메신저 RNA’ 또는 mRNA라고 불러.
mRNA가 떠다닐 때마다 세포는 그것을 읽고 지시에 따라 해당 단백질을 만들어. 유전자, mRNA, 단백질이라는 이 순서는 모든 세포에서 단백질 생산이 이루어지고 통제되는 방식이야. 너무나 근본적이어서 때로는 ‘생물학의 중심 원리’라고 불리기도 해.
누가 나쁜 놈일까?
이들 중 누가 나쁜 놈일까? 헌팅턴병을 연구하는 대부분의 과학자들은 헌팅턴병 돌연변이를 가진 사람들의 세포에서 발생하는 대부분의 문제는 유전자나 메신저가 아니라 돌연변이 단백질 때문이라고 믿어. 그리고 헌팅턴병 돌연변이를 가진 세포에서 잘못되는 많은 일들에 단백질이 책임이 있다는 엄청난 증거가 있어. 하지만 그게 전부일까?
다른 일부 유전 질환에서는 메신저 분자 자체가 문제의 주요 원인이야. 한 가지 예는 근긴장성 이영양증이라는 질병인데, 이 역시 세 글자 유전 서열의 너무 많은 반복으로 인해 발생해. 근긴장성 이영양증에서는 긴 반복을 가진 메시지 분자가 세포를 잘못 작동하게 하고 결국 죽게 만들어. 즉, 해당 단백질이 아니라 mRNA가 문제인 거야.
오랫동안 헌팅턴병에서도 메신저가 해로울 수 있다고 믿는 과학자 그룹이 있었어. 스페인 연구팀의 새로운 연구는 이러한 틀을 깨는 연구자들이 뭔가 중요한 것을 발견했을 수도 있음을 시사해.
세포에서의 초기 연구
2012년, 바르셀로나 대학의 Eulalia Marti가 이끄는 연구팀은 헌팅턴병 유전자 메신저에 대한 매우 흥미로운 연구를 발표했어. 그들은 돌연변이 헌팅턴병 유전자(헌팅턴병이 발병하는 사람들에게서 발견되는 종류)에서 나온 메신저 분자가 실험실에서 배양되는 세포에 독성을 가질 수 있다는 것을 발견했어. 정상 유전자에서 나온 메신저 분자는 세포에 독성이 없었어.
그들이 연구하던 메신저 분자가 실제로 세포에 돌연변이 단백질을 만들라고 지시할 수 없도록 팀이 주의를 기울였기 때문에 이는 놀라운 일이었어. 그들은 또한 몇 가지 상세한 후속 실험을 수행하여 메신저가 독성을 띠게 하는 세포 내 주요 인자들을 밝혀냈어.
하지만 접시 안의 세포에서 어떤 일이 일어날 수 있다고 해서 살아있는 뇌에서도 일어난다는 의미는 아니기 때문에, Marti 팀은 다음으로 헌팅턴병 쥐 모델과 실제 헌팅턴병 환자의 뇌로 관심을 돌렸어. 쥐와 사람의 뇌에서 병든 부위에서 그들은 헌팅턴병 유전자 메신저 분자의 독성 조각들의 증거를 발견했어. 그들이 이 실제 뇌에서 모든 단백질과 다른 물질들을 조심스럽게 제거하고 메신저 분자만 남겼을 때, 이 메신저 분자들이 실험실의 건강한 세포들을 병들게 한다는 것을 발견했어.
이는 헌팅턴병 유전자의 메신저 분자에서 흥미로운 일이 일어나고 있다는 꽤 좋은 증거이며, 헌팅턴병에서 세포가 병드는 일부 이유가 돌연변이 단백질 외의 다른 것들 때문일 가능성이 매우 높다는 것을 보여줘.
“이 새로운 연구는 메신저가 해로울 수 있고, 그 해로움이 중요할 수 있다는 것을 보여주는 영리한 방법을 사용했어.”
쥐를 이용한 새로운 연구
최근 Marti 팀은 그들이 중요한 것을 발견했을 수도 있음을 시사하는 매우 흥미로운 후속 연구를 발표했어. 이 새로운 연구는 메신저가 해로울 수 있고, 그 해로움이 중요할 수 있다는 것을 보여주는 영리한 방법을 사용했어.
Marti와 그녀의 팀은 헌팅턴병 유전자 메신저 분자가 독성을 띠는 것을 막는 방법을 고안했는데, 이는 헌팅턴병 유전자에서 만들어지는 단백질의 수준을 변경하지 않고 이루어졌어. 다시 말해, 메신저는 여전히 존재하며 단백질 생성 기계에 의해 읽힐 수 있지만, 더 이상 직접적으로 해를 끼칠 수는 없어.
놀랍게도 그들은 안티센스 올리고뉴클레오타이드, 즉 ASO라고 불리는 것을 사용하여 바로 이 일을 할 수 있는 방법을 발견했어.
만약 ASO에 이미 익숙하다면, 아마도 그것들이 현재 헌팅턴병 환자들에게 잠재적인 치료법으로 시험되고 있기 때문일 거야. 일반적으로 ASO의 역할은 세포 안으로 들어가 메신저 분자에 달라붙는 것이야.
Ionis Pharmaceuticals에서 만든, 현재 인간에게 시험 중인 ASO는 헌팅턴병 유전자 메신저 분자에 달라붙어 파괴를 목표로 해. 메시지가 적으면 단백질도 적어지고, 우리는 이것이 세포를 해로부터 보호할 것이라고 기대해. 이 접근법은 헌팅틴 감소 또는 때로는 유전자 침묵이라고 불려.
하지만 Marti와 그녀의 동료들이 사용한 ASO는 미묘하게 다른 방식으로 작동해. 그것들은 세포 안으로 들어가 헌팅턴병 메신저 분자를 찾지만, 일단 찾으면 그냥 거기에 달라붙어 머물러. 헌팅턴병 메신저의 파괴는 없고, 따라서 메시지에서 사용되는 단백질 수준의 변화도 없어.
왜 우리는 그렇게 쓸모없는 ASO를 원할까? 왜냐하면 Marti 팀은 헌팅턴병 유전자 메시지에 결합함으로써, 그들이 이전 연구에서 밝혀냈던 메시지의 독성 효과가 차단된다는 것을 발견했기 때문이야. 요컨대, 그들은 헌팅턴병 유전자 메신저가 수행하는 역할의 중요성을 시험할 수 있는 아주 멋진 도구를 발견한 거야.
그들이 이 특별한 ASO를 헌팅턴병 모델 쥐의 뇌에 주입했을 때, 예상했던 대로 독성 메신저 효과는 감소했지만 헌팅턴병 단백질에는 변화가 없었어. 놀랍게도, 여전히 많은 돌연변이 헌팅턴병 단백질이 존재함에도 불구하고 쥐들이 훨씬 더 건강하게 행동한다는 것을 발견했어.
이게 다 무슨 의미일까?
이건 정말 멋진 과학이야. 왜냐하면 매우 신중하게 수행되었고, 헌팅턴병이 어떻게 작동하는지에 대한 우리의 가정을 계속해서 의심해야 한다는 것을 상기시켜 주기 때문이야. 헌팅턴병처럼 복잡한 문제는 여러 원인을 가질 가능성이 높고, 돌연변이 유전자에서 생성된 메신저와 단백질 모두 독성을 가질 수 있다는 것은 전적으로 합리적이야.
이것이 헌팅턴병 치료법, 특히 현재 진행 중인 ASO의 헌팅틴 감소 임상 시험에 어떤 의미일까? 아직 확실하지는 않지만, 직관적으로 Ionis에서 시험 중인 유형의 ASO가 메시지로 인한 독성 효과와 단백질로 인한 독성 효과 모두에 유익할 것이라는 점은 타당해. 헌팅틴 감소를 위한 다른 많은 접근법들도 독성 메신저와 단백질을 제거할 것으로 예상돼. 그리고 미래의 어떤 치료법이 단백질 수준만 ‘단지’ 감소시킨다고 해도, 우리는 그것이 정말 좋은 일일 것이라고 꽤 확신해. 다행이야!
이제 Marti와 그녀의 팀이 길을 보여주었으니, 미래의 연구자들은 새로운 제안된 치료법이 헌팅턴병 돌연변이로 인한 두 가지 가능한 독성 유형에 어떻게 영향을 미치는지 확인할 수 있을 거야.



